Stabilní izotopy v ekologii rostlin
Základy problematiky, trocha teorie
Izotopy (nuklidy) daného prvku mají stejný počet elektronů a protonů, liší se však v počtu neutronů v jádře. Radioizotopy se za určitých podmínek rozpadají, emitují záření a přeměňují se. Stabilní izotopy se nerozpadají. Těžší izotopy jsou většinou vzácnější (výjimka je např. lithium nebo bor). Izotopy mají shodné chemické vlastnosti, ale rozdíl ve hmotnosti dovoluje fyzikálním, chemickým a biologickým procesům zvýhodňovat jeden z izotopů, čímž předávají environmentální signál (McCarroll&Loader, 2004).
| Prvek | Izotop | Abundance v % |
|---|---|---|
| vodík | 1H | 99,985 |
| 2H | 0,015 | |
| uhlík | 12C | 98,982 |
| 13C | 1,018 | |
| dusík | 14N | 99,633 |
| 15N | 0,366 | |
| kyslík | 16O | 99,759 |
| 17O | 0,037 | |
| 18O | 0,204 |
tabulka 1 Přehled výskytu jednotlivých stabilních izotopů vybraných prvků
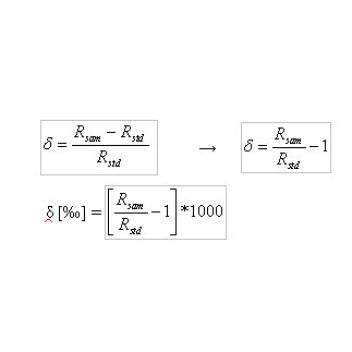
Poměr těžšího izotopu k lehčímu se označuje R (R 13C = 13C/12C). Izotopové složení vzorku se vyjadřuje jako relativní odchylka poměru těžšího a lehčího izotopu ve vzorku a standardu k poměru těžšího a lehčího izotopu ve standardu viz rovnice 1.
Izotopový efekt (α) je způsoben rozdílnými fyzikálními nebo chemickými vlastnostmi, které vyplývají z rozdílů v atomové hmotnosti. Jedná se o kinetický izotopový efekt a rovnovážný izotopový efekt. Kinetický izotopový efekt je spojen s nepřímými, ireverzibilními procesy jako je evaporace, difuse, disociační reakce. Je následkem různých rychlostí přesunu různých izotopomerů (např. 12CO2 nebo 13CO2). Rovnovážný (termodynamický) izotopový efekt je způsoben vlivem hmotnosti na termodynamické vlastnosti molekul, tzn.vliv hmotnosti na pevnost vazeb v chemické sloučenině. Molekuly obsahující těžký izotop jsou stabilnější než molekuly s lehkým izotopem.
Pro izotopové složení se v mnoha biologických pracích používá termín izotopová diskriminace. Pro lepší porovnávání vzorků mezi sebou bylo zavedeno vyjadřování izotopové diskriminace pomocí Δ. Její výhodou je, že je nezávislá na standardu a je možné ji použít při sériových pokusech viz rovnice 2.
Pro studie, kde se používá obohacený materiál (přidání značkovací substance tzv. traceru), se rovnice modifikuje, protože izotopové složení se vymyká jakékoli přirozené úrovni, používá se k vyjádření "atomové procento" (A b ), které je definováno jako A b = Xheavy/(Xheavy + Xlight) = 100*(Rsample/(Rsample + 1))
Studie na úrovni rostlin
Studie zaměřené na rostlinu jako jednotku, která roste v určitých podmínkách a potřebuje využívat jisté zdroje, které zároveň limitují její růst, přežití a výskyt – tyto studie se zaměřují nejčastěji právě na vodu, uhlík a dusík.
Uhlík
Rostliny využívají různé fotosyntetické cesty poutání uhlíku. Zdrojem uhlíku pro fotosyntetické procesy je oxid uhličitý ze vzduchu. Poměr izotopu 13C ke 12C v oxidu uhličitém ve vzduchu v současné době představuje hodnotu δ13C okolo -8 ‰. Míra ochuzení atmosférického CO2 se zvyšuje díky spalování fosilních paliv a odlesňování.
Rostlinná biomasa nabývá hodnot izotopového signálu v určitém intervalu v závislosti na mechanismu fotosyntézy. Hodnoty pro CAM a C3 rostliny leží v intervalu okolo 15 až 25 ‰ (nebo –20 až –35 ‰ při použití vyjádření pomocí δ13C), u C4 rostlin, kde je prvním produktem fotosyntézy čtyřuhlíkatá sloučenina, leží hodnoty mezi 2,5 a 5 ‰ (-11 až –15 s použitím δ13C).
Tato změna v izotopovém poměru mezi zdrojem a produktem je označována termínem frakcionace a stupeň frakcionace je závislý na velikosti (míře) reakce rostliny na podmínky prostředí. Mechanismus diskriminace 13C/12C je vysvětlen teoreticky (Farquhar et al., 1982) a pro C3 rostliny může být vyjádřen jako: Δ ‰ = a + (b - a)(ci/ca),
kde a je diskriminace 13CO2 během difuse skrz průduchy (~ 4,4 ‰), b je čistá diskriminace při karboxylaci (~ 27 ‰) a ci a ca je koncentrace CO2 v intercelulárních prostorech a v atmosféře (Farquhar et al., 1982; McCarroll & Loader, 2004).
Světlo, vzdušná vlhkost, srážky a teplota jsou environmentální faktory známé svým vlivem na fotosyntézu díky svému vlivu na stomatální vodivost a fixaci CO2. Nepřímo ovlivňují signál δ13C v krátkém (cukry, škrob) nebo v dlouhém (rostlinné tkáně, letokruhy) časovém intervalu. Z tohoto důvodu se velmi často používá hodnota δ13C letokruhů k rekonstrukcím klimatu.
Již samotný rozdíl v hodnotách izotopového signálu C3 a C4 nabízí prostor pro nesčetné archeologické / paleozemědělské aj. studie (např. studium δ13C lidského kolagenu ukázalo, že se pěstování kukuřice (C4 rostlina) rozšířilo ze střední Ameriky do Jižní a centrální Severní Ameriky kolem roku 1000 n.l.; stejně tak se dá třeba z exkrementů velkých savců žijících v savaně pozorovat, jak se mění složení potravy v závislosti na sezóně atd.)
Vodík a kyslík
Rostlina přijímá vodu kořeny nebo z okolního prostředí celým povrchem (vodní rostliny). Během příjmu k frakcionaci nedochází a voda v rostlině má shodný signál se zdrojovou vodou; k frakcionaci dochází při výparu a proto jsou výparná místa v listu obohacena až o 50 ‰ proti vodě ve stonku.
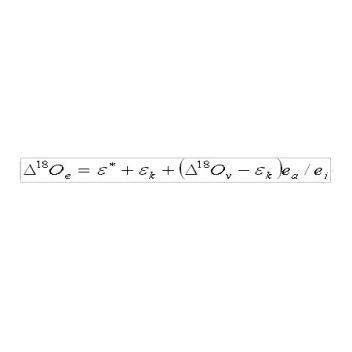
Míra obohacení vody v listu ze zdrojové vody na místě výparu (Δ18Oe ) je dána vztahem (viz rovnice 3), kde ε* je rovnovážný izotopový efekt frakcionace vody (je poměrem izotopových poměrů těžších a lehčích izotopů v kapalné a plynné fázi (ε*= Rkapal/Rplyn), εk je kinetický efekt, tedy frakcionace vody difusí přes stomata a hraniční listovou vrstvu, Δ18Ov je izotopové složení vodních par v atmosféře (vyjádřeno relativně vzhledem ke zdrojové vodě; Δ18Ov= Ratm/Rzdroj -1) a ea a e jsou tlaky vodní páry v atmosféře (vně listu) a v intercelulárním prostoru uvnitř listu, přičemž platí, že δ18Oe > δ18O vody v listu (Pécletův efekt).
K frakcionaci může docházet i vlivem solí rozpuštěných ve vodě. Sladká voda je v porovnání s mořskou ochuzena o deuterium a v pobřežních oblastech je pak možné sledovat, který zdroj vody využívají pobřežní rostliny v jaké míře (většina tropických a subtropických dřevin využívá srážkovou nebo odtokovou vodu).
Analýzy stabilních izotopů vodíku a kyslíku se v současné době hojně využívají ke zjišťování a zlepšování našich vědomostí o vodním provozu rostlin a příklady ukazují, jak mohou různé rostlinné druhy využívat zdroje vody v čase a prostoru. Úspěšně se používají při určení závislosti druhu na povrchové či spodní půdní vodě, povrchovém odtoku / proudící vodě nebo půdní vodě, zimních srážkách nebo mlze či monzunových deštích. Stejně tak se používají analýzy δD a δ18O k odlišení zdroje vody u různých druhů v rámci společenství rostlin na stanovišti nebo se využívají ke zjišťování změn zóny, ze které rostliny berou vodu během vegetačního období tam, kde půdní vlhkost v různých hloubkách během sezóny kolísá. Jde o studie značného významu, protože kořeny často prokořeňují celý půdní profil, ale přítomnost kořenů v určité hloubce neznamená vždy, že tyto kořeny se aktivně podílí na příjmu vody.
Izotopovou analýzu 18O/16O v letokruzích dřevin lze využít k rekonstrukci klimatu – vlhkosti vzduchu i teplot. Nejnovější studie se zaměřují na zkoumání δD a δ18O v půdě, rostlinách a výparu a používají se k vysvětlení úlohy rostlin v procesech na úrovni povodí či v hydrologickém cyklu samotném.
Symbióza rostlin a mykorhizních hub
Rostliny poskytují uhlíkaté sloučeniny houbám, houby zase pomáhají rostlinám získat některé živiny z půdy. Protože spojení mezi kořeny rostlin a houbami se dají dost špatně pozorovat a protože mnoho hub není hostitelsky specifických, houby mohou dostávat uhlíkaté sloučeniny od několika různých hostitelů, stejně jako rostlina může dostávat dusík od řady různých symbiotických hub.
Právě při pozorování, zkoumání a popisování složitých symbiotických vztahů jsou experimenty se značkovacími látkami v podobě těžších izotopů velkým pomocníkem.
Trofické vztahy
Některé studie ukazují na potravní vztahy například mezi mravenci a jejich hostitelskými rostlinami, kde mravenci poskytují rostlinám dusík a získávají uhlíkaté produkty. Některé příklady trofických studií již byly zmíněny výše.
Závěr
Díky mnoha studiím v tomto oboru udělalo naše vědění o světě rostlin a jejich fungování v přirozených podmínkách, a to i v paleontologickém kontextu, veliký pokrok a ukazuje se, že použití metod stabilních izotopů v ekologii rostlin přináší celou řadu výhod.
Dawson T.E., Mambelli S., Plamboeck A.H., Templer P.H., Tu K.P. 2002. Stable isotopes in plant ecology. Annual Review of Ecology Systematics 33: 507-59.
autor:
Autorka je doktorandkou na České zemědělské univerzitě v Praze a externí spolupracovnice Environmentálního informačního centra Domažlice.
Diskuze k článku „Stabilní izotopy v ekologii rostlin“